مقایسه مالئیک انیدرید، اسید مالئیک و اسید فوماریک
مالئیک انیدرید (1)، اسید مالئیک (2) و اسید فوماریک (3) واسطههای شیمیایی چند منظورهای هستند که تقریباً در همه زمینههای شیمی صنعتی کاربرد دارند. هر مولکول شامل دو گروه کربونیل اسیدی و یک پیوند دوگانه در موقعیت a ،b است.
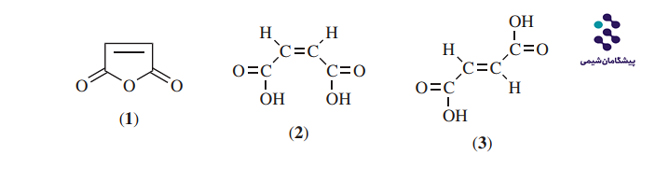
مقایسه اسید فوماریک و اسید مالئیک
مالئیک انیدرید و اسید مالئیک از مواد اولیه مهمی هستند که در ساخت رزینهای آلکیدی و پلی استر از نوع فتالیک، پوششهای سطحی، افزودنیهای روانکننده، نرمکنندهها (qv)، کوپلیمرها (qv) و مواد شیمیایی کشاورزی استفاده میشوند. هر دو ماده شیمیایی نام مشترک خود را از اسید مالیک موجود در طبیعت گرفتهاند.
اسید فوماریک به طور طبیعی در بسیاری از گیاهان وجود دارد و نام آن از شاهتره (نام علمی: Fumaria officinalis)، یک گیاه صعودی یکساله است، گرفته شده است. این ماده به عنوان یک ترکیب اسیدی غذایی و به عنوان یک ماده اولیه در ساخت رزینهای پلی استر غیر اشباع، جوهرهای سریعگیر، لاک مبلمان، مواد شیمیایی تعیین اندازه کاغذ و اسید آسپارتیک استفاده میشود.
تاریخچه
مالئیک انیدرید و دو ایزومر دی اسید برای اولین بار در دهه 1830 آماده شدند اما تولید تجاری تا یک قرن بعد آغاز نشد. در سال 1933، یک شرکت شیمیایی، فرآیندی را برای تولید مالئیک انیدرید بر اساس اکسیداسیون بنزن با استفاده از کاتالیزور اکسید وانادیوم اجرا کرد.
مالئیک اسید در سال 1928 به صورت تجاری در دسترس بود و تولید اسید فوماریک در سال 1932 با ایزومریزاسیون اسید مالئیک کاتالیز شده با اسید شروع شد.
قدرت اسیدی اسید مالئیک
مالئیک اسید یک اسید دی پروتیک ضعیف است که میتواند به صورت مرحلهای جدا شود. همانطور که اسید با باز قوی تیتر میشود، pH به طور مشخص تغییر میکند و منحنی تیتراسیون 2 مرحلهای ایجاد میشود.
سنتز مالئیک اسید
در صنعت، اسید مالئیک از هیدرولیز از مالئیک انیدرید مشتق میشود. مالئیک انیدرید از بنزن یا بوتان در فرآیند اکسیداسیون تولید میشود.
کاربردهای مالئیک اسید
- مالئیک اسید یک ماده اولیه صنعتی برای تولید گلیوکسیلیک اسید با ازنولیز است.
- مالئیک اسید با کم شدن آب به مالئیک انیدرید، با هیدراتاسیون به اسید مالیک و با هیدروژناسیون به اسید سوکسینیک (اتانول / پالادیوم روی کربن) تبدیل میشود. با تیونیل کلراید یا فسفر پنتاکلراید واکنش داده و کلرید اسید مالئیک را ایجاد میکند (جداسازی کلرید مونو اسید امکان پذیر نیست).
- مالئیک اسید در بسیاری از واکنشهای دیلز – آلدر واکنشدهنده است.
کاربردهای فوماریک اسید
وقتی اسید فوماریک به محصولات غذایی اضافه میشود، با E شماره E297 نشان داده میشود.
زیستشناسی
اسید فوماریک در شاهتره (Fumaria officinalis)، قارچ بولت، گلسنگ و خزه ایسلند یافت میشود.فومارات یک واسطه در چرخه اسید سیتریک است که توسط سلولها برای تولید انرژی به شکل آدنوزین تری فسفات (ATP) از غذا استفاده میشود. از اکسیداسیون آدنیل سوکسینات توسط آنزیم سوکسینات دهیدروژناز تشکیل میشود.
سپس فومارات توسط آنزیم فوماراز به مالات تبدیل میشود. پوست انسان هنگام قرار گرفتن در معرض نور خورشید به طور طبیعی اسید فوماریک تولید میکند. فومارات همچنین محصول جانبی چرخه اوره است.
دارو
گاهی اوقات استرهای اسید فوماریک برای درمان پسوریازیس استفاده میشوند، زیرا پیشنهاد شده است که این بیماری به دلیل اختلال در تولید اسید فوماریک در پوست ایجاد میشود. دوز شروع روزانه 60-105 میلیگرم است که ممکن است به تدریج افزایش یابد تا 1290 میلیگرم در روز برسد.
عوارض جانبی شامل اختلالات کلیوی یا گوارشی، و همچنین قرمزی پوست است. اینها عمدتاً در اثر مصرف بیش از حد ایجاد میشوند. کاهش تعداد گلبولهای سفید خون با استفاده طولانی مدت گزارش شده است.
غذا
فوماریک اسید یک ماده اسیدی در مواد غذایی است که از سال 1946 استفاده میشود زیرا غیر سمی است. این به طور کلی در نوشیدنیها و پودرهای پخت استفاده میشود که برای آنها خلوص مورد نیاز است.
به طور کلی به عنوان جایگزین اسید تارتاریک و گاهی به جای اسید سیتریک، به میزان 1.36 گرم اسید سیتریک به ازای هر 0.91 گرم اسید فوماریک برای طعم مشابه استفاده میشود. همچنین در آبنبات برای افزودن ترشی شبیه به نحوه استفاده از اسید مالیک استفاده میشود.
علم شیمی
فوماریک اسید ارزان است، بنابراین معمولاً به جای تهیه آن خریداری میشود. اولینبار از اسید بروموسوکینیک تهیه شد. سنتز سنتی شامل اکسیداسیون فورفورال (از فرآوری ذرت) با استفاده از کلرات سدیم در حضور کاتالیزور مبتنی بر وانادیوم است.
خواص شیمیایی اسید فوماریک را میتوان از گروههای عاملی تشکیلدهنده آن پیشبینی کرد. این اسید ضعیف یک دیی استر ایجاد میکند، در پیوند دوگانه اضافه میشود و یک دی انوفیل عالی است.
استفادههای دیگر
فوماریک اسید در ساخت رزینهای پلی استر و الکلهای پلی هیدریک و به عنوان مایع استفادهکننده

بهترین خرید اسید فوماریک
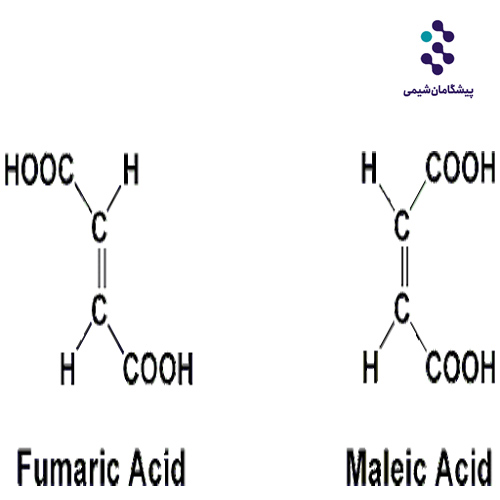
مقایسه اسید فوماریک و اسید مالئیک
تفاوت گرمای احتراق آنها 22.7 کیلوژول بر مول است. خواص فیزیکی اسید مالئیک با اسید فوماریک بسیار متفاوت است.مالئیک اسید در آب محلول است، در حالی که اسید فوماریک اینطور نیست.
و نقطه ذوب اسید مالئیک (130 – 139 درجه سانتیگراد) نیز بسیار کمتر از اسید فوماریک (287 درجه سانتیگراد) است. هر دو خاصیت اسید مالئیک را میتوان با توجه به پیوند هیدروژنی درون مولکولی که به دلیل فعل و انفعالات بین مولکولی صورت میگیرد، توضیح داد.
چرا اسید مالئیک بیشتر از اسید فوماریک اسیدی است؟
- مالئیک اسید سیس- بوتن دیوئیک است در حالی که اسید فوماریک اسید ترانس- بوتن دیوئیک است. مالئیک اسید قادر به از دست دادن یون است و منجر به تشکیل پیوند هیدروژنی درون مولکولی میشود. به همین دلیل است که اسید مالئیک قوی تر از اسید فوماریک است.
- فوماریک اسید که ایزومر ترانس است، کمترین مانع استریکی خواهد داشت زیرا گروههای کربوکسیلیک اسید در طرفهای مختلف پیوندهای دوگانه قرار خواهند گرفت و کمترین دافعه الکترونیکی را ایجاد خواهند کرد. بنابراین در مقایسه با اسید مالئیک پایدارتر خواهد بود.
- مالئیک اسید شامل یک گروه اتیلن است که توسط دو گروه کربوکسیلیک اسید احاطه شده است. مالئیک اسید ایزومر سیس- اسید بوتن دیوئیک است، در حالی که اسید فوماریک ایزومر ترانس است. ایزومر سیس یکی از این دو پایداری کمتری دارد.
واکنش تبدیل مالئیک اسید به اسید فوماریک
ایزومریزاسیون اسید مالئیک و اسید فوماریک در حالت عادی قابل تغییر نیستند زیرا چرخش حول پیوند دوگانه کربن کربن امکانپذیر نیست. در آزمایشگاه، تبدیل ایزومر cis به ایزومر ترانس با استفاده از نور و مقدار کمی برم امکانپذیر است. نور بروم عنصری را به رادیکال برم تبدیل میکند، که در واکنش اضافی رادیکال به رادیکال برومو آلکان به آلکن حمله می کند.
و در این حالت چرخش پیوند منفرد امکانپذیر است. رادیکالهای برم دوباره ترکیب شده و اسید فوماریک تشکیل میشود.در روش دیگری، اسید مالئیک از طریق فرآیند گرم کردن اسید مالئیک در دمای بالا در محلول 12 مولار اسید کلریدریک به اسید فوماریک تبدیل میشود. هنگام گرم شدن مولکول یک مولکول آب را از دست میدهد و تبدیل به یک انیدرید اسید میشود.
هنگامی که حرارت برداشته میشود، انیدرید اسید مولکول آب را پس میگیرد، اما به عنوان اسید فوماریک آپولار تغییر شکل میدهد. به همین دلیل است که از محلول HCl قطبی خارج میشود، زیرا حلال قطبی یک املاح غیر قطبی را حل نمی کند.
در صنعت، اسید فوماریک نیز از اسید مالئیک بوسیله ایزومریزاسیون کاتالیزوری با اسیدهای معدنی، برومات یا تیوره تولید میشود. باز هم تفاوت زیاد در حلالیت در آب تصفیه اسید فوماریک را آسان می کند.






















2 نظر در “مقایسه اسید فوماریک و اسید مالئیک”
باسلام
روز بخیر..
تفاوت اصلی در حلالیت و پایداری بین اسید فوماریک و اسید مالئیک چیست و کدامیک در صنایع غذایی کاربرد بیشتری دارد؟
تفاوت اصلی بین این دو اسید در حلالیت و پایداری ساختاری آنهاست. اسید مالئیک در آب بسیار محلولتر است، درحالیکه اسید فوماریک حلالیت کمتری دارد اما پایدارتر است. در صنایع غذایی، اسید فوماریک بیشتر بهعنوان تنظیمکننده pH و عامل اسیدیکننده در نوشیدنیها و محصولات پودری استفاده میشود، زیرا ماندگاری بیشتری دارد. در مقابل، اسید مالئیک به دلیل حلالیت بالاتر، در برخی کاربردهای خاص مورد استفاده قرار میگیرد اما کمتر از فوماریک رایج است.