خرید نیترات سرب
شرکت بازرگانی پیشگامان شیمی فعال در حوزه فروش نیترات سرب با بهترین کیفیت، و مناسب ترین قیمت در مقادیر آزمایشگاهی و صنعتی به مشتریان می باشد. جهت خرید نیترات سرب چینی و آلمانی (آزمایشگاهی) و دریافت اطلاعات بیشتر درباره قیمت نیترات سرب با ما تماس بگیرید.
نیترات سرب قیمت
شما عزیزان می توانید جهت اطلاعات بیشتر در مورد قیمت نیترات سرب صنعتی و آزمایشگاهی و نحوه خرید به صفحه تماس با ما مراجعه کرده و از طریق فرم یا شماره های موجود در سایت با ما تماس بگیرید.
فروش نیترات سرب
| به انگلیسی | Lead (II) Nitrate |
| فرمول شیمیایی | Pb(NO3)2 |
| وزن مولکولی | 331.21 |
| شکل ظاهری | پودری یا کریستالی سفید |
| خلوص | 99.8 درصد |
| تولید کننده | چین، آلمان |
| محل نگهداری | دمای اتاق |
| قیمت نیترات سرب | لطفا با ما تماس بگیرید |
نیترات سرب چیست
نیترات سرب (II) یک نوع ترکیب معدنی با فرمول شیمیایی Pb(NO3)2 می باشد. این ماده یک پودر سفید یا کریستال بی رنگ بوده و بر عکس سایر نمک های سرب (II)، محلول در آب است. از قرون وسطی این ماده را با نام plumb dulcis می شناسند، از کاربردهای اصلی آن به عنوان ماده اولیه در تولید رنگدانه در رنگ های سربی می توان نام برد. در قرن نوزدهم، فرمولاسیون نیترات سرب II برای اولین بار به صورت تجاری در اروپا و ایالات متحده تولید شد. پایداری پلی استر و نایلون مورد استفاده در پوشش های کاغذ فتوترموگرافی یکی از کاربردهای فراوان آن است.
ساختار نیترات سرب
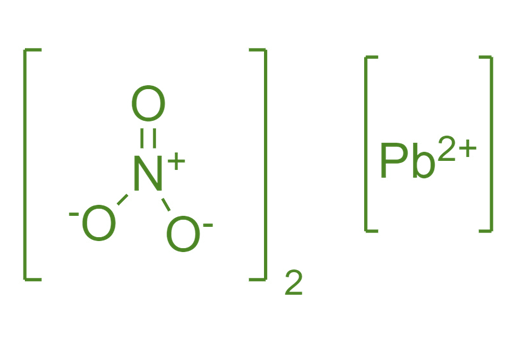
سرب یک فلز واسطه و نیترات از دسته غیرفلزی است. نیترات یک یون چند اتمی است. در نتیجه نیترات سرب (II) تلفیقی از فلزات و غیر فلزات است. (II) نشان می دهد که در نیترات سرب (II)، سرب دارای بار 2+ و نیترات دارای بار 1- است. فرمول نیترات سرب (II) سرب (NO3)2 است که از یک رویکرد متقاطع برای خنثی کردن بار استفاده می کند.
تولید نیترات سرب
این ماده زمانی تشکیل می شود که اکسید سرب (II) با اسید نیتریک قوی واکنش می دهد.
PbO + 2 HNO3 (con.) → Pb(NO3)2 ↓ + H2O
همچنین می توان محلول حاصل از واکنش سرب فلزی با اسید نیتریک ضعیف را تبخیر کرد.
Pb + 4 HNO3 → Pb(NO3)2 + 2 NO2 + 2 H2O
محلول و کریستال های نیترات سرب (II) از تصفیه ضایعات سرب-بیسموت از یک پالایشگاه سرب حاصل می شود. نیترات سرب زمانی تولید می شود که کربنات سرب با اسید نیتریک قوی واکنش می دهد. واکنش به شرح زیر است.
هنگامی که سولفید سرب با اسید نیتریک قوی واکنش می دهد، نیترات سرب را می توان تهیه کرد، واکنش به شرح زیر است
3PbS +8HNO3 → 3Pb(NO3)2 + 3S +2NO + 4H2O
مشخصات فیزیکی
- نیترات سرب (ll) یک جامد سفید کریستالی است که به راحتی در آب حل می شود و یک محلول تقریباً شفاف تشکیل می دهد.
- در دمای صفر درجه سانتیگراد، نیترات سرب (ll) 376.5 گرم در لیتر، 597 گرم در لیتر در 25 درجه سانتیگراد و 127 گرم در لیتر در 100 درجه سانتیگراد حل می شود.
- دارای جرم مولی 331.2 گرم بر مول.
- از نظر ظاهری بی رنگ یا سفید است.
- در آب محلول است.
- نقطه جوش: 83 درجه سانتیگراد
- چگالی 4.53 گرم بر سانتی متر مکعب است.
- سطح Ph 6.5 است.
- دمایی که در آن ذوب می شود 470 درجه سانتیگراد است.
خواص شیمیایی
نیترات سرب (II) با هیدروکسید سدیم برهمکنش میکند و یک رسوب سفید، هیدروکسید سرب (II) تشکیل میدهد.
Pb(NO3)2 + 2NaOH → Pb(OH)2 + 2NaNO3
ابتدا رسوبی از هیدروکسید سرب (II) تشکیل می شود که با هیدروکسید سدیم اضافی حل می شود و به آن آلو سدیم می گویند. یک محلول بی رنگ تشکیل دهید.
واکنش نیترات سرب (II) با محلول یدید پتاسیم، رسوب زرد روشنی از یدید سرب ایجاد می کند.
Pb(NO3)2 + 2KI → PbI2 + 2KNO3
این معمولاً با استفاده از آزمایش باران طلایی معمولی نشان داده می شود که در آن یدید سرب در آب جوش حل می شود و هنگامی که سرد می شود به رنگ طلایی زیبا تبدیل می شود.
نیترات سرب (II) با کرومات پتاسیم واکنش می دهد و یک رسوب زرد رنگ، کرومات سرب (II) تشکیل می دهد.
Pb(NO3)2 + K2CrO4 → 2KNO3 + PbCrO4
نیترات سرب (II) نیز تحت یک واکنش جایگزینی با سولفات آمونیوم قرار می گیرد تا یک رسوب سفید، سولفات سرب را تشکیل دهد.
Pb(NO3)2 + (NH4)2S → PbS + NH4NO3
تجزیه حرارتی نیترات سرب (ll).
در حالی که لوله آزمایش را به صورت مورب نگه می دارید، 1 گرم نیترات سرب (II) در لوله آزمایش روی شعله مشعل Bunsen قرار می گیرد. گرما با. موقعیت پس از مدتی صدای کوبیدن آشنا و به دنبال آن گاز قهوه ای را خواهید شنید.
2Pb(NO3)2 → 2PbO + 4NO2 + O2
پیرولیز نیترات سرب (II) اکسید سرب، دی اکسید نیتروژن (گاز قهوه ای) و گاز اکسیژن تولید می کند.
کاربرد نیترات سرب
- کبریت ها و مواد منفجره ویژه شامل نیترات سرب (II) است.
- در صنعت رنگ و عکاسی استفاده می شود.
- برای حکاکی استفاده می شود.
- همچنین می تواند برای پشتیبانی از فرآیند شستشو در فرآیند سیانیداسیون استفاده شود.
اثرات بهداشتی و خطرات ایمنی
نیترات سرب (II) در طبیعت بسیار سمی است. از طریق خوردن انسان و حیوانات نیز سمی است. به عنوان یک سرطان زا برای انسان طبقه بندی می شود. علاوه بر این، تراتوژن نیز هست.
سوالات متداول
سوال 1: فرآیند حذف نیترات سرب از آب چگونه است؟
راه حل:
تبادل یونی، تقطیر و اسمز معکوس همگی روش های موثری برای حذف نیترات از آب هستند. حذف نیترات از آب با حرارت دادن یا جوشاندن آن غیرممکن است.
سوال 2: فرمول شیمیایی محلول نیترات سرب چیست؟
راه حل:
فرمول شیمیایی نیترات سرب (II) Pb(NO3)2 است. جرم مولی 331.2 گرم بر مول است. این مولکول از یک کاتیون سرب Pb2+ و دو آنیون نیترات NO3- ساخته شده است. با کاتیون سرب، دو آنیون یک اتصال یونی ایجاد می کنند.
سوال 3: در مورد گرم کردن کریستال های نیترات سرب در یک لوله شیشه ای سخت مشاهداتی ارائه دهید.
راه حل:
2Pb(NO3)3 → 2PbO + 4NO2 + O2
هنگامی که کریستال های نیترات سرب گرم می شوند، اکسید سرب تولید می شود که به رنگ زرد است و دی اکسید نیتروژن که به رنگ قرمز مایل به قهوه ای است، منتشر می شود.
سوال 4: واکنش نیترات سرب با یدید پتاسیم
راه حل:
هنگامی که نیترات سرب (آبی) با یدید پتاسیم ترکیب می شود، یون یدید نیترات را از نیترات سرب جابجا می کند و نیترات با پتاسیم برای تولید نیترات پتاسیم واکنش می دهد، در حالی که سرب با ید واکنش می دهد و یدید سرب را تشکیل می دهد. در نتیجه دو ماده شیمیایی تشکیل می شود: یدید سرب، یک جامد زرد رنگ و نیترات پتاسیم.
Pb(NO3)2 (aq) + 2KI (aq) → PbI2 (s) + 2KNO3 (aq)
(جامد زرد)
سوال 5: وقتی نیترات سرب تا دمای بالا گرم می شود، نتیجه چیست؟
راه حل:
2Pb(NO3)2 → 2PbO + 4NO2 + O2
واکنشی که در بالا توضیح داده شد یک واکنش تجزیه است که در آن نیترات سرب (ll) تجزیه می شود. هنگامی که نیترات سرب تا دمای بالا گرم می شود، به اکسید سرب، اکسید نیتروژن و اکسیژن تجزیه می شود. از این واکنش می توان برای تولید گاز دی اکسید نیتروژن نیز استفاده کرد و می توان از آن به عنوان جونده کش استفاده کرد.
منبع:geeksforgeeks




