خرید اسید فسفریک
فروش اسید فسفریک 85 درصد در گالن های 35 کیلویی صورت می گیرد. جهت خرید اسید فسفریک خوراکی و صنعتی و دریافت قیمت اسید فسفریک از واردکننده مستقیم با کارشناسان فروش ما در ارتباط باشید.
جهت دریافت آنالیز
و استعلام قیمت اسید فسفریک
و همچنین دریافت مشاوره رایگان با ما تماس بگیرید.
۰۲۱۵۴۰۳۲۳۱۷
۰۲۱۵۴۰۳۲۳۱۸
۰۹۱۲۹۰۰۸۸۶۲
شنبه تا چهارشنبه ۹ الی ۱۷ | پنج شنبه ۹ الی ۱۳
| ✅ به انگلیسی | Phosphoric-Acid |
| ✅ فرمول شیمیایی | H3PO4 |
| ✅ نام های دیگر | اسید اورتوفسفریک؛ هیدروکسی (اکسو) فسفونیوم، هیپوفسفر اسید |
| ✅ cas No | 7664-38-2 |
| ✅ گرید | غذایی، صنعتی، کشاورزی |
| ✅ شکل محصول | مایع روشن |
| ✅ خلوص | 85% |
| ✅ کاربرد | محصول میانی مهمی در تولید صنعت کودهای شیمیایی، ماده خام فسفات مورد استفاده در صابون، مواد شوینده، عامل تصفیه سطح فلز، افزودنی مواد غذایی، افزودنی خوراک و عامل تصفیه آب است. عامل طعم دهنده: ماده شیرین کننده در نوشیدنی مایع یا جامد و نوشیدنی سرد، جایگزین اسید سیتریک |
| ✅ کشور تولیدی | چین |
| ✅ بسته بندی | گالن 25 کیلویی |
| ✅ محل تحویل | تهران- اصفهان |
| ✅ قیمت | تماس بگیرید 📞 |
اسید فسفریک چیست؟
اسیدفسفریک (Phosphoric acid) به عنوان فسفریک (V) اسید یا اسید ارتو فسفریک نیز نامیده میشود و یکی از اسیدهای محبوب و مورد استفاده است. به این ترتیب، فرم خام این اسید از سنگهای فسفات استخراج میشود، در حالی که فرم با خلوص بیشتری از فسفر سفید به صورت صنعتی تولید میشود.
اسید فسفریک خالص معمولاً به حالت جامد بلوری و به شکل غلیظ است. به طور کلی مایعی بیرنگ، بیبو و غیر فرار است. این ماده که یک اسید معدنی است با فرمول H3PO4 نشان داده میشود و حاوی یک اتم فسفر، چهار اتم اکسیژن و سه اتم هیدروژن است.
جرم مولی اسید فسفریک 99/97 گرم بر مول است. اتم فسفر مرکزی از طریق پیوند دوگانه به یک اتم اکسیژن و از طریق پیوندهای تک به سه گروه هیدروکسیل (-OH) متصل میشود. بنابراین، H3PO4 می تواند حداکثر سه یون +H آزاد کند. این اسید از پرمصرفترین مواد شیمیایی در صنعت است. این ماده در دو نوع صنعتی و خوراکی به کار میرود.
مایعی بیرنگ، شفاف، بیبو و دارای طعم تند است. در نوشابههای گاز دار، تولید کودهای شیمیایی، پاککنندههای صابونی و غیر صابونی، تصفیه آب، خوراک دام و داروسازی، مکملهای غذای دام و طیور، تولید کودهای فسفاته، ضد حریقکردن برخی سطوح و عوامل بازدارنده اشتعال و نیز جهت تمیز کردن و جرمگیری سطوح فلزی به عنوان ماده افزودنی به کار میرود. این اسید با خلوص 85 درصد به بالا خوراکی و زیر 85 درصد صنعتی محسوب میشود.
تهیه اسید فسفریک
فسفریک اسید از طریق فرآیند مرطوب به صورت صنعتی تولید میشود که در آن اسید سولفوریک با آپاتیت (سنگ فسفات تری کلسیم) واکنش نشان میدهد.
Ca5 (PO4) 3Cl + 5 H2SO4 + 10 H2O → 3 H3PO4 + 5 CaSO4 · 2 H2O + HCl
محلول فسفریک حاصل فقط حدود 32-46٪ H3PO4 است، بنابراین با تبخیر آب غلیظ میشود تا گریدهای تجاری اسید فسفریک با غلظت بالاتر تولید کند.
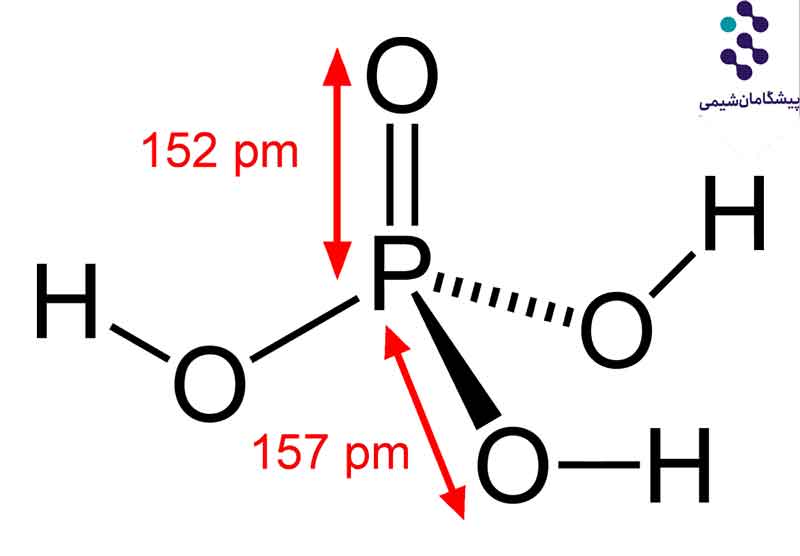
خصوصیات فیزیکی اسید فسفریک
فسفریک خالص یک ماده جامد بلوری سفید با نقطه ذوب 35/42 درجه سانتیگراد است. هنگامی که غلظت کمتری داشته باشد، مایع چسبناک بیرنگ، بدون بو با چگالی 1.885 گرم در میلیلیتر است. غیر سمی و غیر فرار است. متداولترین غلظت این اسید در آب 85٪ است.
خواص شیمیایی اسید فسفریک
این اسید دارای سه اتم اسیدی و قابل تعویض است. بنابراین، واکنش متفاوتی نسبت به سایر اسیدهای معدنی نشان میدهد. میتواند با بازها واکنش داده و با جایگزینی یک، دو یا سه اتم H، به ترتیب NaH2PO4، Na2PO4 و Na3PO4، سه کلاس نمک تشکیل دهد.
در دمای بالا، مولکولهای آن میتوانند با هم واکنش نشان دهند و با ترکیب (با از دست دادن مولکول آب) تشکیل دیمر، تریمر و حتی زنجیرههای پلیمری طولانی مانند اسیدهای پلی فسفریک و اسیدهای متافسفریک را بدهند.
2H3PO4 → H4P2O7 (- H2O)
کاربرد و مصارف اسید فسفریک:
- مواد شوینده مانند تری سدیم فسفات و سدیم تری پلی فسفات
- تولید مواد تصفیهکننده و منعقد کننده در صنعت آب و فاضلاب
- تولید پاککنندههای فسفاته صنعتی و تهیهی نمکهای فسفاته
- صنایع غذایی به صورت گرید خوراکی
- اسید فسفریک کشاورزی در تولید کود مانند کودهای فسفاتدار مانند در امونیوم فسفات و …
- در پزشکی و دندانپزشکی به عنوان زبر کردن سطح دندان و عامل قلمزنی جهت تمیز کردن
- زدودن زنگ آهن
- کشاورزی (پسته، از فاکتورهای مهم و اساسی برای جذب مواد غذایی در درختان)
- صنعت آبکاری
علاوه بر این، این اسید یک ترکیب در استخوان و دندان است و در بسیاری از فرآیندهای متابولیک نقش دارد. فسفریک اسید در چندین مایع بیولوژیکی مانند مدفوع، ادرار و خون شناسایی شده است. درون سلول، این اسید در درجه اول در سیتوپلاسم قرار دارد.
اسید فسفریک در همه یوکاریوتها، از مخمر گرفته تا انسان وجود دارد. در انسان، این اسید در مسیر متابولیسم گلوتامات، متابولیسم گلوتاتیون، فسفات گلیسرول و مسیر متابولیسم پورین نقش دارد.

اسید فسفریک مورد استفاده برای از بین بردن زنگزدگی
در میان انواع مختلف اسیدها، از فسفریک معمولاً برای از بین بردن زنگ زدگی از فلزات مانند آهن، فولاد و غیره استفاده میشود. معمولاً وقتی از این اسید استفاده میشود با زنگ زدگی واکنش نشان میدهد و آهن قهوهای مایل به قرمز به طور معمول اکسید فریک (اکسید آهن) را به یک ترکیب سیاه رنگ که اکنون فسفات فریک است، تبدیل میکند. این ماده به راحتی از بین میرود.
اسید فسفریک خوراکی در مواد غذایی و آشامیدنی
این اسید اغلب به عنوان افزودنی غذایی استفاده میشود. این اسید به عنوان تنظیم کننده اسیدیته در غذاهایی مانند مربا، میله غلات، گوشتهای فرآوری شده، پنیر و… عمل میکند.
در صنعت نوشیدنی، از آن به عنوان یک ماده اسیدی استفاده میشود. این ترکیب به شما کمک میکند تا قارچها و تشکیل باکتریها را بررسی کنید. همچنین به طعم این نوشیدنیها میافزاید. با این حال، بحث در مورد اثرات و فواید این اسید بر سلامتی ادامه دارد.
اسید فسفریک مورد استفاده در محصولات مراقبت شخصی
اسید فسفریـک در تولید طیف گستردهای از محصولات مراقبت شخصی کاملاً لازم است. برخی از آنها شامل محصولات پاککننده، محصولات حمام، رایحه، محصولات مراقبت از مو و رنگ، محصولات ناخن، آرایش و سایر محصولات مراقبت از پوست است. از طرف دیگر، این اسید نیز در کنترل سطح pH این محصولات استفاده میشود.
اسید فسفریک مورد استفاده در کشاورزی
برخی گزارشها حاکی از آن است که تقریباً 80 درصد فسفریک تولید شده در تولید کود مصرف میشود. همچنین به عنوان ماده افزودنی و طعمدهنده در خوراک دام یا طیور استفاده میشود.
اسید فسفریک مورد استفاده در داروسازی
این اسید بیشتر به عنوان واسطه در داروسازی استفاده میشود. یکی از زمینههای اصلی استفاده از آن در دندانپزشکی است. این ماده به عنوان محلول اچ استفاده میشود و معمولاً برای تمیز کردن دندانها کاربرد دارد.
از دیگر کاربردهای اسید فسفریـک میتوان به سفید کننده دندان یا مایعات شستشوی دهان اشاره کرد. اسید فسفریـک معمولاً در داروهای ضد تهوع استفاده میشود.
سایر کاربردها
این اسید کاربردهای دیگری نیز دارد. به عنوان الکترولیت در سلولهای سوختی یا در مولدهای اکسی هیدروژن وبرای ساخت مواد شوینده مصنوعی و تصفیه آب و فلزات استفاده میشود.
این ماده همچنین برای از بین بردن رسوبات معدنی، لکههای سیمان و لکههای آب سخت در صنعت ساختمان استفاده میشود. این ترکیب میتواند به عنوان یک ماده اکسید کننده شیمیایی برای تولید محصولات کربن فعال عمل کند.
نکاتی در مورد اسید فسفریک
در صورت تماس با پوست باعث قرمز شدن و درد و تاول پوست میشود. تماس با چشم باعث قرمزی، درد، کدر شدن میدان دید و سوختگی شدید و عمیق میشود.
گوارشی: سوزش، گیجی، تنگی تنفس، زخم گلو، بیهوشی و ضعف میشود. نباید با فلزات، آلدئیهها، سیانیدها، مرگاپتانها، سولنیدها تماس داشته باشد.
خطرات بهداشتی، اثرات سلامتی
اسید فسفریک سمی یا خطرناک در نظر گرفته نمیشود. در غلظتهای کم، روی پوست و برای مصرف بیخطر است (در محصولات غذایی، آرایشی و بهداشتی و دندان استفاده میشود). با این حال، در غلظتهای بسیار بالا، خورنده است و میتواند باعث سوختگی پوست شود.
قیمت اسید فسفریک صنعتی
قیمت اسید فسفریک صنعتی، خوراکی و آزمایشگاهی با توجه به وارداتی بودن این محصول تابعی از نرخ ارز و هزینه های حمل و نقل و تعرفه گمرکی می باشد. جهت دریافت قیمت روز و قیمت اسید فسفریک کشاورزی می توانید در زیر برای ما پیغام بگذارید. در ایران این محصول توسط پتروشیمی رازی نیز تولید می شود که می توانید استعلام قیمت اسید فسفریک پتروشیمی رازی (کارخانه واقع در بندر امام) که در بورس نیز عرضه می شود، را نیز از ما داشته باشید.
اسید فسفریک از کجا بخریم؟
خرید اسید فسفریک 85 درصد در بستهبندیهای 20 لیتری (35 کیلوگرمی) و مخازن 1000 لیتری و به صورت پلمپ را از ما انجام دهید. شرکت پیشگامان شیمی آمادگی دارد ضمن دریافت سفارش شما مشتریان عزیز، محصول اسیدفسفریک مورد نیاز صنایع غذایی و دارویی را با بهترین قیمت و کیفیت تأمین کرده و در اسرع وقت به وسیله سیستم حملونقل مطمئن به شهرهای مختلف ارسال نماید.
آنالیز اسید فسفریک:
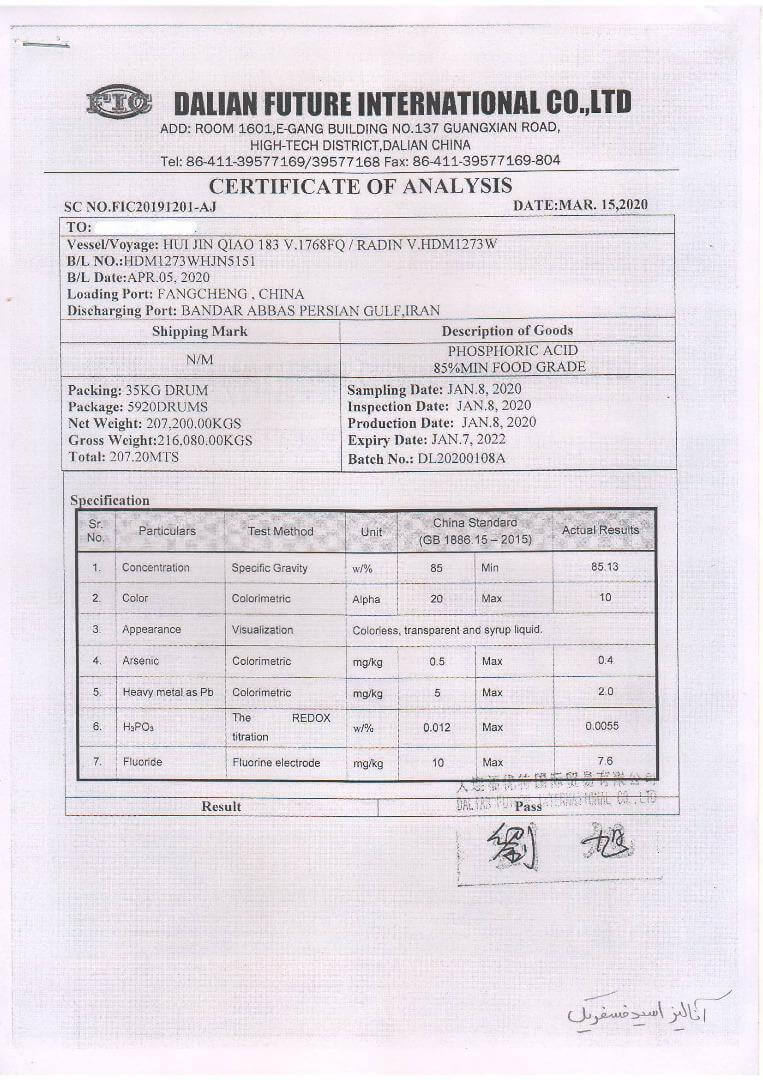
جهت دریافت آنالیز جدیدتر نوع مایع و پودری با کارشناسان فروش ما تماس بگیرید.
فروش عمده اسید فسفریک
اسید فسفریک صنعتی ایرانی و چینی به صورت عمده با بهترین قیمت را از ما بخواهید. این شرکت با داشتن نمایندگی در مشهد، شیراز، یزد، تهران و اصفهان بهترین شرایط را برای خرید بی دردسر برای شما مهیا کرده است.
سوالات متداول درباره اسید فسفریک
تفاوت اسید فسفریک خوراکی و صنعتی چیست
اسید فسفریک به سه دسته خوراکی، صنعتی و خام تقسیم می شود. اسید فسفریک صنعتی در تولید ظروف تفلون، مواد شوینده و در منسوجات استفاده می شود. اسید فسفریک خوراکی در تولید روغن های گیاهی، خوراک دام و مکمل های خوراک دام استفاده می شود.
اسید فسفریک خوراکی چیست
اسید فسفریک گرید غذایی مایعی شفاف، بی بو و کمی چسبناک است. اسید فسفریک درجه غذایی برای اسیدی کردن غذاها و نوشیدنی ها مانند انواع نوشابه ها و مرباها استفاده می شود. طعمی تند یا ترش می دهد.
آیا اسید فسفریک در مواد غذایی بی خطر است؟
اسید فسفریک به طور کلی توسط سازمان غذا و داروی ایالات متحده به عنوان ایمن یا GRAS شناخته می شود. آیا می توان از اسید فسفریک در غذاهای ارگانیک، گیاهی، حلال یا کوشر به بازار استفاده کرد؟ بله، اسید فسفریک را می توان در محصولاتی که برچسب گیاهخواری دارند استفاده کرد.
آیا اسید فسفریک برای انسان مضر است؟
اسید فسفریک می تواند ریه ها را تحریک کند. مواجهه مکرر ممکن است باعث ایجاد برونشیت همراه با سرفه، خلط و/یا تنگی نفس شود. قرار گرفتن طولانی مدت در معرض مایع ممکن است باعث خشک شدن و ترک خوردن پوست شود.
آیا اسید فسفریک برای شما مفید است؟
اسید فسفریک از ماده معدنی فسفر ساخته می شود که به طور طبیعی در بسیاری از غذاها یافت می شود. به گفته مؤسسه ملی بهداشت، این ماده با کلسیم برای تشکیل استخوانها و دندانهای قوی کار میکند. همچنین به حمایت از عملکرد کلیه و نحوه استفاده و ذخیره انرژی بدن شما کمک می کند.
اسید فسفریک چقدر سمی است؟
تماس باعث سوختگی شدید همراه با قرمزی، تورم، درد و تاری دید می شود. آسیب دائمی از جمله کوری می تواند منجر شود. بلع: می تواند لب ها، زبان، گلو و معده را بسوزاند. علائم ممکن است شامل تهوع، استفراغ، گرفتگی معده و اسهال باشد.
آیا قهوه حاوی اسید فسفریک است؟
در قهوه، اسید فسفریک تقریباً کمتر از 1٪ ماده خشک قهوه را تشکیل می دهد و اعتقاد بر این است که از هیدرولیز اسید فیتیک از خاک سرچشمه می گیرد. با این حال، بر خلاف برخی از اسیدهای دیگر - فسفر قوی ترین است و به راحتی می تواند 100 برابر قوی تر از اسیدهای دیگر باشد.
آیا اسپرایت حاوی اسید فسفریک است؟
دو اسید رایج مورد استفاده در نوشابه ها اسید سیتریک و اسید فسفریک هستند. اسید سیتریک در نوشابه های با طعم مرکبات مانند Sprite، Crush و Mountain Dew یافت می شود. اسید فسفریک در نوشابه های تیره تر مانند کولا یافت می شود و مضرتر از این دو اسید است.
چه مقدار اسید فسفریک در نوشابه وجود دارد؟
نوشیدنی های کولا حاوی 50 تا 70 میلی گرم اسید فسفریک در 100 میلی لیتر هستند.
اسید فسفریک عمدتاً برای چه مواردی استفاده می شود؟
اسید فسفریک جزء کودها (80 درصد کل مصرف)، مواد شوینده و بسیاری از محصولات پاک کننده خانگی است. محلول های رقیق طعم اسیدی دلپذیری دارند. بنابراین، از آن به عنوان یک افزودنی غذایی نیز استفاده می شود و خواص اسیدی را به نوشابه ها و سایر غذاهای آماده و در محصولات تصفیه آب می دهد.
آیا اسید فسفریک باعث پوسیدگی دندان می شود؟
نوشابه همچنین حاوی اسید فسفریک است که برای دندان ها بسیار خورنده است. برای اینکه بفهمید چقدر فرساینده است: از اسید فسفریک در کودها و جلا دادن فلزات نیز استفاده می شود. حتی مقادیر کم آن می تواند مینای دندان شما را فرسایش دهد.
اسید فسفریک کجا یافت می شود؟
اسید فسفریک یک مایع بی رنگ، بی بو و کریستالی است که حاوی عنصر فسفر است و در بسیاری از نوشابه های گازدار شیرین یا نوشابه های گازدار یافت می شود.
آیا اسید فسفریک اسید قوی است؟
اسید فسفریک یک اسید ضعیف با فرمول شیمیایی H3PO4 است. اسید فسفریک یک اسید حاوی چهار اتم اکسیژن، یک اتم فسفر و سه اتم هیدروژن است. همچنین به نام اسید فسفریک (V) یا اسید اورتوفسفریک نیز شناخته می شود.
اسید فسفریک 85 درصد برای چه مواردی استفاده می شود؟
اسید فسفریک به طور معمول برای کنترل pH در صنایع غذایی استفاده می شود، به عنوان مثال در ساخت محصولات پنیر، چربی ها و شورتنینگ ها. همچنین در صنعت نوشابه سازی در نوشابه ها به ویژه کولا استفاده می شود.
آیا اسید فسفریک برای پوست بی خطر است؟
قرار گرفتن در معرض کوتاه مدت: اسید فسفریک جامد یا محلول های آن ممکن است باعث سوختگی پوست شود. تماس با چشم ممکن است باعث سوزش و سوختگی چشم شود. قرار گرفتن در معرض بخار اسید فسفریک یا غبار ممکن است باعث تحریک چشم، بینی و گلو شود.



2 دیدگاه. ارسال دیدگاه جدید
سلام و وقت بخیر. ممنون از مطلب مفیدتون. چندتا سوال داشتم. اول اینکه امکان ارسال اسید فسفریک رو دارید؟ من برای کار آزمایشگاهی دنبال این اسید هستم و خواستم از کیفیت محصول مطمئن بشم. سایت های زیادی رو گشتم و متاسفانه چون نمیشه در خرید اینترنتی کیفیت محصول رو متوجه شد، خواستم از کیفیت بالای بسته بندی و نحوه ارسال اسید مطمئن بشم و بعد خرید کنم. توی سایت های خوبی که این محصول رو می فروشن، سایت شما تاکید زیادی به درصد خلوص محصول داشت و همین مساله مد نظر مجموعه ماست. سوال دیگه اینکه چطور می تونیم سفارشمون رو ثبت کنیم؟
سایت بسیار خوب و مفیدی بود. ممنون از شما. موفق باشید.