خرید سولفیت سدیم خوراکی
جهت خرید و استعلام قیمت سولفیت سدیم صنعتی و خوراکی با کارشناسان ما تماس بگیرید. خرید آنلاین سولفیت سدیم E221 با بهترین قیمت به دلیل واردات مستقیم از کشور چین را از ما تجربه کنید.
جهت دریافت آنالیز
و استعلام قیمت سولفیت سدیم خوراکی و صنعتی
و همچنین دریافت مشاوره رایگان با ما تماس بگیرید.
۰۲۱۵۴۰۳۲۳۱۷
۰۲۱۵۴۰۳۲۳۱۸
۰۹۱۲۹۰۰۸۸۶۲
شنبه تا چهارشنبه ۹ الی ۱۷ | پنج شنبه ۹ الی ۱۳
سولفیت سدیم چیست
سولفیت سدیم نمکی غیر آلی با فرمول شیمیایی Na2SO3 است. این یک ترکیب یونی است که شامل دو کاتیون سدیم (+Na) و یک آنیون سولفیت (–SO32) است. یک محلول اشباع شده از سولفیت سدیم در آب باز ضعیفی است و مقدار pH تقریبی آن 9 است. چنین محلولی میتواند متبلور شود تا بلورهای هپتاهیدرات Na2SO3 بدست آورد. سولفیت سدیم یک نمک سدیم محلول سولفوریک اسید (سولفیت) با فرمول شیمیایی Na2SO3 است.
سولفیت سدیم در شکل بیآب آن، یک ماده جامد سفید است که دارای املاح کم است. همچنین دارای فعالیتهای سفید کننده، سولفوریزهکردن و دفعکننده است. تفاوت اصلی بین Na2SO3 بیآب و هپتاهیدرات آن ثبات نسبی فرم بیآب نسبت به اکسیداسیون است. Na2SO3.7H2O به آهستگی توسط اکسیژن اتمسفر اکسید میشود و باعث ایجاد سولفات مربوطه میشود.
ساختار سولفیت سدیم
در یک مولکول سولفیت سدیم، دو پیوند یونی بین کاتیونهای سدیم و آنیون سولفیت وجود دارد. ساختار یک مولکول Na2SO3 در زیر نشان داده شده است.
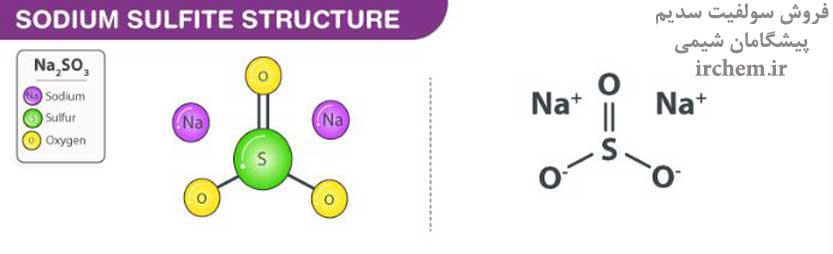
هر یون سدیم دارای بار 1 + است. از طرف دیگر، 2- بار بر روی یون سولفیت به دلیل رزونانس از محل خارج میشود، و در نتیجه یک بار جزئی ⅔- بر روی هر اتم اکسیژن ایجاد میشود. بار کلی مولکول Na2SO3 صفر است.
خواص سدیم سولفیت
برخی از خصوصیات مهم فیزیکی و شیمیایی سولفیت سدیم در این بخش ذکر شده است.
خواص فیزیکی سدیم سولفیت
سولفیتسدیم یک سدیم معدنی حاوی سولفیت است. این ماده بهعنوان نگهدارنده غذا و عامل کاهشدهنده کلر استخر نقش دارد. این ماده دارای چگالی g / cm3 2.633 بوده، نسبتاً سمی و محلول در آب است و به آرامی تجزیه میشود.سولفیت سدیم در آب حل میشود، اما حلالیت آن در الکل کمتر است. این ماده بهعنوان نگهدارنده برای توسعهدهندههای قلیایی و بهعنوان یک عامل تصفیهکننده در چاپ عکاسی استفاده میشود. سولفیت سدیم صنعتی با واکنش گاز دی اکسید گوگرد با محلول هیدروکسید سدیم یا کربنات سدیم تهیه میشود.
خنثیسازی بیشتر با هیدروکسید سدیم در حالی که دمای بالاتر از 33.6 درجه سانتیگراد را حفظ میکند منجر به کریستالشدن سولفیتسدیم بیآب میشود.
شکل هپتاهیدرات دارای چگالی نسبتاً کمتری برابر با 1.561 گرم در سانتی متر مکعب است.با گرم شدن تا K 306.5 (33.4oC)، هپتاهیدرات دچار کم آبی میشود. فرم بی آب در دمای o 500 ذوب میشود.سولفیت سدیم نقطه جوش خاصی ندارد زیرا در دمای بالا تمایل به تجزیه دارد.
این ماده در آب به صورت متوسط قابل حل است، حلالیت آن برابر با 27 گرم در 100 میلی لیتر است.ساختار بلوری Na2SO3 بیآب شش ضلعی است در حالی که بلورهای هپتاهیدرات ساختاری مونوکلینیک دارند.

خواص شیمیایی سولفیت سدیم
در اثر تماس با اسیدهای قوی یا ضعیف، Na2SO3 تجزیه میشود و دی اکسید گوگرد گازی را آزاد میکند.سولفیت سدیم با آلدئیدها واکنش داده و یک ترکیب اضافی بیسولفیت تولید میکند. با این حال، اسید سولفونیک از واکنش آن با کتونها تولید میشود. محلولهای سولفیت سدیم توسط اکسیژن اتمسفر اکسید شده و سولفات سدیم تولید میکند.
این ترکیب در آمونیاک و کلر نامحلول است.این ماده به راحتی اکسید شده است به طور گستردهای بهعنوان یک عامل کاهشدهنده مناسب استفاده میشود. این ماده از واکنش دیاکسید گوگرد با کربناتسدیم یا هیدروکسید سدیم تهیه میشود. اسیدهای معدنی تجزیه میشود و پروتئین دیاکسید گوگرد را آزاد میکند.سولفیتسدیم یک عامل کاهشدهنده است، به ویژه در شرایط اساسی. با عوامل اکسیدکننده مانند پراکسید، اپوکسیدها، اکسواسیدها واكنش میدهد.
سولفیت سدیم اسید است یا باز؟
سولفیت سدیم، Na2SO3، نمکی است که از واکنش خنثیسازی بین یک باز قوی (هیدروکسید سدیم) و یک اسید ضعیف (اسید سولفور) ساخته میشود. بنابراین محلول آبی آن ماهیت کاملاً بازی دارد و مقدار pH آن کمی بیشتر از 7 است.
آماده سازی سولفیت سدیم
- در آزمایشگاهها، سولفیت سدیم به طور کلی از واکنش بین دی اکسید گوگرد گازی (SO2) و هیدروکسید سدیم (NaOH) تهیه میشود. معادله شیمیایی این واکنش توسط
SO2 + 2NaOH → Na2SO3 + H2O
کاهش واکنش دهنده NaOH را میتوان با افزودن چند قطره H2SO4 غلیظ، و در نتیجه آزاد سازی گاز SO2 تشخیص داد.
- از نظر صنعتی، Na2SO3 از واکنش بین دی اکسید گوگرد و محلول کربنات سدیم تولید میشود. در ابتدا بی سولفیت سدیم (NaHSO3) تشکیل میشود. این ترکیب اکنون با کربنات سدیم یا هیدروکسید سدیم واکنش داده و محصول سولفیت سدیم را بدست میآورد. واکنش را میتوان به موارد زیر تعمیم داد:
Na2CO3 + SO2 → Na2SO3 + CO2
کاربرد سولفیت سدیم
بهعنوان ماده سازنده در تولید پارچه و کاغذ استفاده میشود. سدیم بعضی اوقات بهعنوان نگهدارندههای بیولوژیکی استفاده میشود.این ماده یک ماده نگهدارنده موثر ضد میکروبی، به خصوص در برابر قارچها در pH پایین (w/v 0.1٪) از سولفیت سدیم خوراکی استفاده میشود. این ماده در :
- مواد آرایشی
- مواد غذایی
- بهعنوان نگهدارنده مواد غذایی برای گوشت، زرده تخممرغ و… مورد استفاده قرار میگیرد.
- داروهای کاربردی مانند:
-
- فرمولاسیونهای تزریقی
- استنشاق
- فرمولاسیون دهان
- آمادهسازی موضعی
استفاده میشود.
- سولفیت سدیم صنعتی همچنین به طور عمده در صنعت عکاسی استفاده میشود، برای:
- نقاشی و تولید هیدرو سولفیت سدیم
- سفید کردن الیاف نساجی
- خرید سدیم سولفید صنعتی بهعنوان یک کاهشدهنده در رنگهای تولیدی
- بهعنوان حذف Cl در پارچههای سفید و کاغذ
خرید سولفیت سدیم خوراکی که کاربردهای بیشمار دیگری دارد که در زیر لیست شده است.
- این ترکیب اغلب برای جلوگیری از تغییر رنگ میوههای خشک و حفظ گوشت استفاده میشود زیرا میتواند به عنوان ماده نگهدارنده عمل کند.
- این ماده همچنین در استخرها برای کاهش سطح کلر در آب استفاده میشود.
- در سیستمهای دیگ بخار، این ترکیب به عنوان یک جاذب اکسیژن برای محافظت از سیستم در برابر خوردگی حفرهای عمل می کند. بنابراین، آب تغذیه شده به دیگهای بخار اغلب با سولفیت سدیم تصفیه میشود.
- صنعت نساجی استفاده گستردهای از Na2SO3 برای اهداف سفید سازی، دکلره و گوگردزدایی میکند.
- سولفیت سدیم همچنین در فرآیند خالصسازی تری نیتروتولوئن (TNT) به منظور مناسب ساختن آن برای استفاده نظامی استفاده میشود.
- سولفیتسدیم جزء بسیاری از داروهاست که برای حفظ قدرت و ثبات داروها موثر است. همچنین میتواند برای تصفیه آب بهعنوان عامل جذبکننده اکسیژن مورد استفاده قرار گیرد.
خطرات بهداشتی سولفیت سدیم
سولفیتها ترکیباتی حاوی یون سولفیت هستند، که اغلب در ترکیب با سدیم (سولفیت سدیم) یا پتاسیم (سولفیت پتاسیم) هستند. سولفیتها گاز تحریک کننده دی اکسید گوگرد را آزاد میکنند که به عنوان ماده نگهدارنده و سفید کننده عمل میکند.
سولفیتها علاوه بر اینکه به طور طبیعی در برخی غذاها و بدن انسان دیده میشوند، به برخی مواد غذایی اضافه میشوند تا به عنوان ماده نگهدارنده عمل کنند زیرا از رشد میکروبی جلوگیری میکنند، رنگ غذا را حفظ میکنند و ماندگاری را افزایش میدهند.غذاهایی که معمولاً سولفیت به آنها اضافه میشود شامل شراب، آبجو و میوههای خشک است. همچنین از آنها برای سفید کردن نشاستههای غذایی مانند نشاسته سیب زمینی استفاده میشود و در تولید برخی از مواد بستهبندی مواد غذایی مانند سلفون استفاده میشود.
آلرژی سولفیت سدیم
هنوز مشخص نیست که چرا سولفیتها در برخی افراد واکنش آلرژیک ایجاد میکنند اما در برخی دیگر این واکنش را نشان نمیدهد. دی اکسید گوگرد یک گاز تحریک کننده است و بنابراین انقباض رفلکس مجاری تنفسی به عنوان یک مکانیسم ممکن پیشنهاد شده است، زیرا اکثر افراد آلرژیک به سولفیت علائم شبه آسم را از خود نشان میدهند.
فروش سولفیت سدیم خوراکی
فروش سولفیت سدیم و فروش متابی سولفیت سدیم خوراکی، در کیسههای 25 کیلوگرمی آماده تحویل به شما مشتریان عزیز میباشد. شرکت پیشگامان شیمی آمادگی دارد ضمن دریافت سفارشهای مشتریان عزیز، محصول سولفیت سدیم مورد نیاز صنایع غذایی و دارویی را بهترین قیمت سولفیت سدیم صنعتی و کیفیت تأمین کرده و در اسرع وقت به وسیله سیستم حملونقل مطمئن به شهرهای مختلف ارسال نماید.
پودر سولفیت سدیم از کجا بخریم
جهت خرید سولفیت سدیم 97% فوق خالص بی آب ترمو ساینتیفیک با بالاترین کیفیت در بسته بندی های 25 کیلوگرمی با ما تماس بگیرید. این شرکت وارد کننده سولفیت سدیم با بهترین قیمت رقابتی می باشد.


